ما هي الكيمياء الذرية؟ دليل شامل لفهم بنية الذرة وأسرارها
ملاحظة تحريرية: يقدّم هذا المقال معلومات علمية مبسطة حول ما هي الكيمياء الذرية بلغة دقيقة وواضحة، مع تجنب الادعاءات غير المثبتة والاعتماد على المفاهيم الأساسية المعروفة في علم الكيمياء.
ما هي الكيمياء الذرية؟ إنها الفرع الذي يدرس الذرة بوصفها الوحدة الأساسية للمادة، ويهتم بفهم بنيتها الداخلية، وطبيعة مكوناتها، وكيف تؤثر هذه البنية في خواص العناصر وتفاعلاتها الكيميائية. وعندما يسأل القارئ ما هي الكيمياء الذرية فهو في الحقيقة يقترب من أحد أهم المفاتيح التي تشرح لماذا تختلف المواد عن بعضها، ولماذا يتصرف كل عنصر بطريقة مميزة على المستوى الكيميائي.
تكمن أهمية هذا المجال في أنه يربط بين العالم غير المرئي الذي تتكون منه المادة وبين الظواهر التي نلاحظها يوميًا، مثل الاحتراق، والصدأ، وتكوّن المركبات، وتوصيل الكهرباء، وحتى بعض التطبيقات الطبية والصناعية الحديثة. لذلك فإن فهم الكيمياء الذرية لا يقتصر على الدراسة الأكاديمية فقط، بل يساعد أيضًا على بناء تصور أعمق لكيفية تنظيم المادة في الطبيعة.
ما المقصود بالكيمياء الذرية؟
الكيمياء الذرية هي المجال الذي يركز على دراسة الذرات من حيث بنيتها ومكوناتها وسلوكها وعلاقتها بخصائص العناصر. وهي تبحث في النواة، والبروتونات، والنيوترونات، والإلكترونات، ومستويات الطاقة، وكيف تؤثر هذه العناصر كلها في تكوين الروابط والتفاعلات الكيميائية.
وبعبارة أبسط، إذا كانت الكيمياء العامة تشرح لنا كيف تتفاعل المواد، فإن الكيمياء الذرية تساعدنا على فهم السبب العميق وراء هذه التفاعلات. فهي تفسر لماذا يرتبط عنصر بآخر، ولماذا يكون بعض العناصر أكثر نشاطًا، ولماذا تختلف خواص المواد على الرغم من أن جميعها مكونة في النهاية من ذرات.
ما هي الذرة ولماذا تعد أساس المادة؟
الذرة هي أصغر وحدة من العنصر يمكنها أن تحتفظ بخصائصه الكيميائية. وهذا يعني أن ذرة الحديد ما تزال تمثل الحديد، وذرة الأكسجين ما تزال تمثل الأكسجين، حتى لو لم تكن مرئية بالعين المجردة. وتتكون الذرة من نواة مركزية صغيرة وكثيفة تضم البروتونات والنيوترونات، بينما تتحرك الإلكترونات حولها في مناطق طاقة محددة.
تكمن روعة هذا البناء في أن معظم حجم الذرة فراغ نسبيًا، لكن توزيع الشحنات والجسيمات داخلها هو الذي يحدد سلوكها الكيميائي. ومن هنا تبدأ الكيمياء الذرية في تفسير كيف يمكن لبنية صغيرة جدًا كهذه أن تكون مسؤولة عن تنوع هائل في المواد والخواص والتفاعلات.
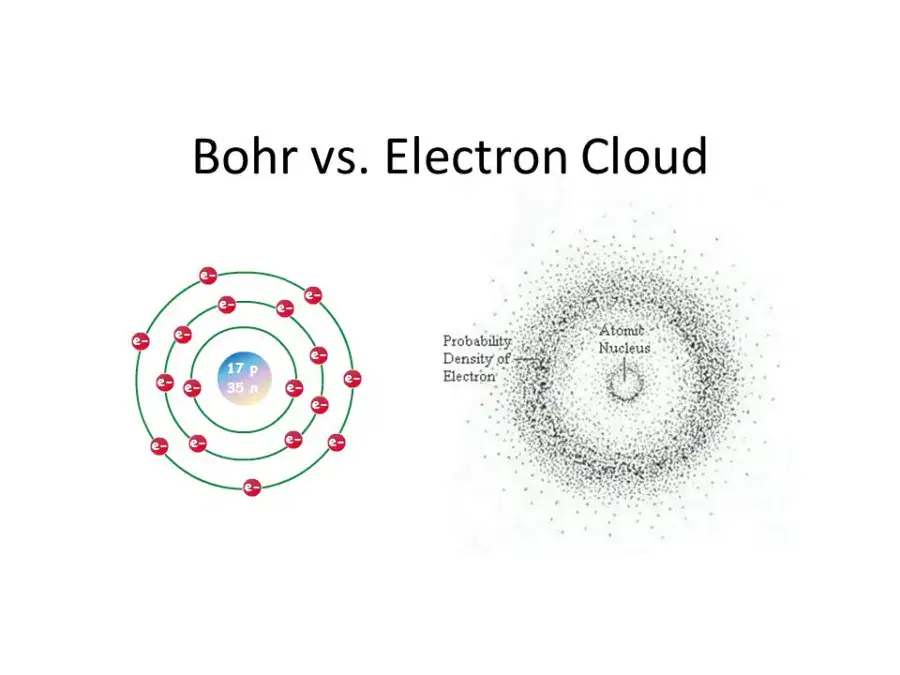
مكونات الذرة الأساسية
البروتونات
البروتونات جسيمات موجبة الشحنة توجد داخل النواة، وعددها هو الذي يحدد هوية العنصر. فالعدد الذري لأي عنصر يساوي عدد البروتونات في نواته، ولهذا السبب يُعد هذا العدد بطاقة التعريف الأساسية لكل عنصر في الجدول الدوري.
النيوترونات
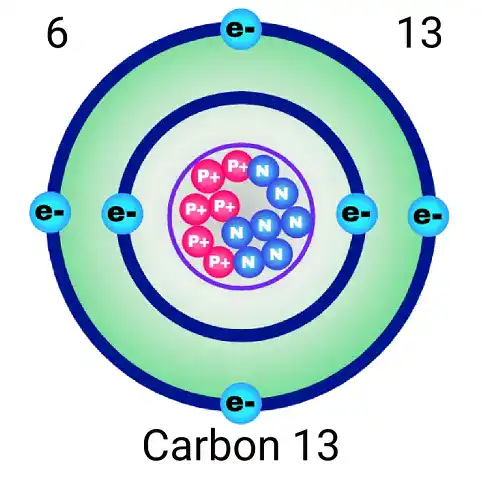
النيوترونات جسيمات متعادلة الشحنة توجد أيضًا في النواة، وتؤثر في الكتلة والاستقرار النووي. وقد يختلف عدد النيوترونات بين ذرات العنصر نفسه، وهو ما يؤدي إلى ظهور النظائر.
الإلكترونات
الإلكترونات جسيمات سالبة الشحنة تتحرك حول النواة في مستويات أو مدارات طاقة. وهذه الإلكترونات، خصوصًا الموجودة في المستوى الخارجي، هي التي تحدد كيفية تفاعل الذرة مع غيرها، وبالتالي تحدد أغلب السلوك الكيميائي للعناصر.
كيف تفسر الكيمياء الذرية اختلاف العناصر؟
يفسر هذا العلم اختلاف العناصر من خلال الاختلاف في عدد البروتونات والإلكترونات وطريقة توزيع الإلكترونات حول النواة. فالعنصر الذي يملك إلكترونات خارجية قليلة قد يفقدها بسهولة، بينما عنصر آخر قد يميل إلى اكتساب إلكترونات أو مشاركتها في الروابط الكيميائية.
وهذا التوزيع الإلكتروني هو المفتاح لفهم الجدول الدوري نفسه. فترتيب العناصر في الجدول لا يعتمد على الكتلة فقط، بل على العدد الذري والبنية الإلكترونية، وهو ما يفسر التشابه بين مجموعات معينة من العناصر واختلافها عن غيرها.
العلاقة بين الكيمياء الذرية والروابط الكيميائية
لا يمكن فهم الروابط الكيميائية جيدًا دون المرور عبر ما هي الكيمياء الذرية. فعندما تتفاعل الذرات، فإنها لا تتعامل عبر النواة مباشرة، بل من خلال إلكتروناتها الخارجية. وهذه الإلكترونات قد تُنقل من ذرة إلى أخرى، أو تُشارك بين ذرتين، أو تتوزع بطريقة تؤدي إلى تكوين أنواع مختلفة من الروابط.
ومن هنا نفهم لماذا تتكون المركبات، ولماذا تختلف في الثبات والصلابة والذوبان والتوصيل الكهربائي. فكل هذه الصفات ترتبط بطريقة اتحاد الذرات، وهذه الطريقة بدورها ترتبط بالبنية الذرية لكل عنصر مشارك في التفاعل.
ما أهمية مستويات الطاقة والإلكترونات الخارجية؟
تحتل الإلكترونات مواقع طاقة مختلفة حول النواة، ولا تتوزع بشكل عشوائي. وكل مستوى من هذه المستويات يحدد مقدار الطاقة التي يحملها الإلكترون وموقعه التقريبي. والإلكترونات الخارجية، أو إلكترونات التكافؤ، هي الأهم في الكيمياء لأنها تدخل مباشرة في التفاعلات.
وعندما تمتلئ بعض المستويات أو تقترب من الامتلاء، يتغير سلوك الذرة بشكل واضح. ولهذا السبب تظهر بعض العناصر مستقرة نسبيًا، بينما تبدو عناصر أخرى أكثر ميلًا إلى التفاعل. وهذه الفكرة من أهم الأفكار التي تجعل الكيمياء الذرية أداة تفسيرية قوية في العلوم.
ما دور النظائر في الكيمياء الذرية؟
النظائر هي ذرات للعنصر نفسه تمتلك العدد نفسه من البروتونات، لكنها تختلف في عدد النيوترونات. وهذا يعني أنها تنتمي إلى العنصر ذاته كيميائيًا، لكنها قد تختلف في بعض الخصائص الفيزيائية مثل الكتلة والاستقرار. وتُعد النظائر من الموضوعات المهمة في الكيمياء الذرية لأنها تربط بين بنية النواة والتطبيقات العملية.
وتظهر أهمية النظائر في مجالات متعددة، مثل البحث العلمي، والتطبيقات الطبية، وتتبع بعض العمليات الطبيعية والكيميائية. وهي مثال واضح على أن التغير البسيط داخل النواة قد يؤدي إلى نتائج مهمة في الاستخدام والتفسير.
كيف تطورت فكرة الذرة عبر الزمن؟
لم تظهر صورة الذرة الحديثة دفعة واحدة، بل تطورت عبر مراحل علمية متعددة. بدأت الفكرة القديمة على أنها تصور فلسفي عن وجود وحدات صغيرة جدًا من المادة، ثم تحولت مع الزمن إلى نماذج علمية قائمة على التجربة والملاحظة. ومع التقدم في الفيزياء والكيمياء، أصبح العلماء أكثر قدرة على فهم النواة والإلكترونات ومستويات الطاقة.
وقد ساعد هذا التطور على نقل الذرة من فكرة نظرية بسيطة إلى مفهوم علمي دقيق نسبيًا، يفسر كثيرًا من خصائص المادة. وهذا يوضح أن الكيمياء الذرية ليست مجرد معلومات ثابتة، بل نتيجة تراكم علمي طويل ساعد على بناء فهمنا الحالي للمادة.
تطبيقات الكيمياء الذرية في الحياة والعلوم
قد يبدو هذا المجال نظريًا للوهلة الأولى، لكنه حاضر في تطبيقات كثيرة. ففهم الذرات أساسي في تصميم المواد الجديدة، وتطوير الصناعات الكيميائية، وفهم خواص المعادن والبلاستيك والزجاج والمواد الموصلة. كما أن بعض التطبيقات الطبية والبحثية تعتمد على معرفة دقيقة بالبنية الذرية والنظائر.
وتظهر أهميته أيضًا في التعليم، لأن كثيرًا من فروع الكيمياء والفيزياء لا يمكن فهمها بعمق من دون أساس ذري واضح. لذلك فإن من يسأل ما هي الكيمياء الذرية يفتح الباب أمام فهم أوسع للعلوم الطبيعية كلها تقريبًا.
جدول يوضح أهم مفاهيم الكيمياء الذرية
| المفهوم | المعنى المبسط | الأهمية |
|---|---|---|
| الذرة | أصغر وحدة من العنصر تحتفظ بخصائصه | الأساس البنيوي للمادة |
| البروتون | جسيم موجب داخل النواة | يحدد هوية العنصر |
| النيوترون | جسيم متعادل داخل النواة | يسهم في الكتلة والاستقرار |
| الإلكترون | جسيم سالب حول النواة | يؤثر في التفاعل الكيميائي |
| إلكترونات التكافؤ | الإلكترونات الخارجية في الذرة | تحكم تكوين الروابط |
| النظائر | ذرات للعنصر نفسه تختلف في عدد النيوترونات | مهمة في التطبيقات العلمية والطبية |
لماذا تعد الكيمياء الذرية مهمة للطلاب والمبتدئين؟
لأنها تبني الأساس الذي يعتمد عليه فهم موضوعات كثيرة لاحقًا، مثل الروابط الكيميائية، والتفاعلات، والجدول الدوري، والخواص الفيزيائية والكيميائية للعناصر والمركبات. وعندما يفهم الطالب بنية الذرة جيدًا، يصبح من السهل عليه ربط كثير من المعلومات التي كانت تبدو منفصلة أو صعبة.
كما أن هذا المجال يعلّم طريقة التفكير العلمي نفسها: كيف نفسر الظواهر الكبيرة من خلال وحدات صغيرة جدًا، وكيف نقيم العلاقات بين البنية والسلوك. وهذا يجعل الكيمياء الذرية ليست مجرد فصل دراسي، بل أداة ذهنية لفهم المادة من أساسها.
الأسئلة الشائعة حول ما هي الكيمياء الذرية
ما هي الكيمياء الذرية باختصار؟
هي فرع من الكيمياء يدرس الذرة من حيث مكوناتها وبنيتها وتوزيع إلكتروناتها، ويشرح كيف تؤثر هذه البنية في خصائص العناصر وتفاعلاتها.
ما الفرق بين الكيمياء الذرية والكيمياء العامة؟
الكيمياء العامة تشرح التفاعلات والمواد بشكل أوسع، بينما تركز الكيمياء الذرية على البنية الداخلية للذرة والأساس الذي تنتج عنه تلك التفاعلات والخصائص.
لماذا الإلكترونات مهمة جدًا في الكيمياء الذرية؟
لأن الإلكترونات، خصوصًا الخارجية منها، هي المسؤولة عن تكوين الروابط الكيميائية وتحديد كيفية تفاعل الذرات مع بعضها.
هل للكيمياء الذرية تطبيقات عملية فعلًا؟
نعم، فهي تدخل في فهم المواد، والصناعات الكيميائية، وبعض التطبيقات الطبية والبحثية، كما تشكل أساسًا مهمًا لكثير من العلوم الحديثة.
فهم الذرة هو بداية فهم المادة
إن سؤال ما هي الكيمياء الذرية يقود مباشرة إلى واحد من أهم أبواب العلم، لأنه يفتح الطريق لفهم المادة من جذورها الدقيقة. فمن خلال دراسة الذرة ومكوناتها وتوزيع إلكتروناتها، يصبح من الممكن تفسير كثير من الظواهر الكيميائية التي تبدو معقدة على السطح.
ولهذا تبقى الكيمياء الذرية مجالًا أساسيًا لكل من يريد فهم العناصر والروابط والتفاعلات بطريقة أعمق. إنها ليست مجرد حديث عن جسيمات صغيرة جدًا، بل شرح لكيفية بناء العالم المادي من وحدات دقيقة تتحكم في تنوعه وخصائصه الهائلة.
✍️ عن المراجعة التحريرية والخبرة
خضع هذا المحتوى لمراجعة تحريرية متخصصة، بالاعتماد على مصادر موثوقة ومراجع معتمدة في هذا المجال. نحرص على تقديم معلومات واضحة ومتوازنة تساعد القارئ على الفهم دون تهويل أو جزم.
اقرأ في مقالنا عن:
- ما هي الكيمياء الحيوية؟ دليل شامل لفهم كيمياء الحياة
- الهندسة الوراثية البشرية: علاج الأمراض أم بداية الأطفال المصممين
- ما هي الكيمياء التحليلية؟ دليل شامل لتعريفها وتطبيقاتها اليومية
- ما هي الكيمياء الفيزيائية؟ دليل شامل لفهم فروعها وتطبيقاتها
- ما هو القانون العلمي؟ أمثلة مبسطة على أشهر القوانين العلمية
- أقطاب المغناطيس: شرح مبسط لماذا تتجاذب الأقطاب وتتنافر
- الابتكارات في علاج الأمراض المزمنة: تقنيات حديثة في علاج الأمراض المزمنة
المراجع والمصادر الخارجية
- Encyclopaedia Britannica, دون تاريخ. Atom | Definition, Structure, History, Examples, Diagram, & Facts – Britannica.
- Encyclopaedia Britannica, دون تاريخ. Atomic model | Definition, History, Development, Examples, & Facts – Britannica.
- Khan Academy, دون تاريخ. Atomic structure – Khan Academy.
الذرة: بنيتها الداخلية، خصائصها التعريفية، وتفاعلاتها الكيميائية